
Was das Gehirn der KI beibringen kann
Haben Sie sich jemals gefragt, warum selbst die modernste künstliche Intelligenz nicht an die Lernfähigkeit eines menschlichen Gehirns heranreicht? Die Antwort liegt in einem revolutionären Ansatz, der Biologie und Technologie verbindet: NeuroAI. Diese Disziplin nutzt Erkenntnisse aus der Neurowissenschaft, um Maschinen intelligenter, adaptiver und menschlicher zu gestalten.
Unser Gehirn ist seit Millionen von Jahren optimiert – ein Vorbild, das Algorithmen völlig neue Wege zeigt. Wie genau übersetzen Forscher biologische Prinzipien in Code? Und warum wird diese Symbiose aus Gehirn und KI zum Gamechanger für Industrie und Medizin?
Wir zeigen Ihnen, wie NeuroAI internationale Forschungsprojekte antreibt. Von der Nachbildung neuronaler Netzwerke bis zu selbstlernenden Systemen, die Fehler korrigieren wie ein Mensch. Entscheidungsträger erhalten hier Einblicke, wie diese Technologien Märkte transformieren – und warum frühes Verständnis entscheidend ist.
Schlüsselerkenntnisse
- NeuroAI verbindet Neurowissenschaft mit KI-Entwicklung
- Das menschliche Gehirn dient als Blaupause für adaptive Algorithmen
- Internationale Forschungsteams treiben technologische Quantensprünge voran
- Biologisches Lernen inspiriert selbstoptimierende KI-Systeme
- Frühzeitige Kenntnisse sichern Wettbewerbsvorteile in der Anwendung
Einführung: Die Synergie von Gehirn und KI

Die Fusion von Biologie und Technik schafft neue Potenziale für maschinelles Lernen. Unser Gehirn verarbeitet Informationen mit beispielloser Effizienz – ein Prinzip, das Forscher jetzt in Algorithmen übersetzen. Diese Brücke zwischen Neurowissenschaft und KI entwickelt sich zum Schlüssel für adaptive Systeme, die wie Menschen aus Erfahrungen lernen.
Grundlagen der Neurowissenschaft und maschinelles Lernen
Neuronale Netzwerke imitieren die Vernetzung von Gehirnzellen. Doch echte Innovation entsteht, wenn Forschung biologische Lernmechanismen decodiert. Ein Beispiel: Dopamin-gesteuerte Belohnungssysteme inspirieren Reinforcement-Learning-Algorithmen. So entstehen KI-Modelle, die Entscheidungen nicht nur berechnen, sondern bewerten.
Bedeutung der Interaktion zwischen biologischen und künstlichen Systemen
Internationale Projekte wie das Human Brain Project zeigen: Je genauer wir natürliche Lernprozesse verstehen, desto leistungsfähiger werden digitale Lösungen. Krankenhäuser nutzen bereits NeuroAI-Systeme, die MRT-Daten in Echtzeit analysieren – ein direkter Transfer neurowissenschaftlicher Erkenntnisse.
Die Zukunft liegt in dieser Symbiose. Wer heute die Systeme von morgen gestalten will, muss beide Welten verbinden. Denn erst das Zusammenspiel von Gehirn und Code ermöglicht KI, die nicht repliziert, sondern wirklich versteht.
Technologische Grundlagen und Modelle in NeuroAI

Moderne KI-Systeme orientieren sich an der Effizienz biologischer Lernprozesse. Forscher entwickeln neuronale Netzwerke, die nicht nur Daten verarbeiten, sondern Muster erkennen wie unser Gehirn. Diese Architekturen bilden das Fundament für intelligente Modelle, die sich selbst optimieren.
Neuronale Netzwerke und Deep Learning Ansätze
Künstliche Neuronen imitieren synaptische Verbindungen. Doch erst Deep Learning ermöglicht komplexe Analysen. Ein Beispiel: Transformer-Architekturen verarbeiten Sprache in Schichten – ähnlich wie Hirnareale visuelle Reize deuten.
Praxisanwendungen zeigen das Potenzial:
- Medizinische Bilderkennung mit 94% Genauigkeit durch 3D-Netzwerke
- Echtzeit-Übersetzungssysteme mit adaptiven Attention-Mechanismen
- Autonome Roboter, die durch Trial-and-Error lernen
Modellierung von Gehirnfunktionen mit Machine Learning
Wie entstehen aus Forschungsdaten nutzbare Modelle? Das EU-Projekt “Human Brain Simulation” zeigt es: Maschine-Learning-Algorithmen kartieren 86 Milliarden Nervenzellen. Sie analysieren Stoffwechselprozesse und übertragen sie auf energieeffiziente KI-Chips.
Ein Durchbruch gelang bei der Vision. NeuroAI-Systeme erkennen Objekte jetzt kontextabhängig – nicht durch reines Pixel-Scannen. Diese Technologie revolutioniert Sicherheitssysteme und medizinische Diagnostik gleichermaßen.
Anwendungen in klinischer Forschung und Pharmatechnologie

Wie revolutioniert moderne Bildgebung die Medikamentenforschung? Neuroimaging wird zum Gamechanger – es liefert Einblicke in Gehirnprozesse, die früher unmöglich waren. Diese Technologien beschleunigen die Entwicklung neuer Therapien und sparen Millionen ein.
Vom Labor zur klinischen Praxis
Führende Pharmaunternehmen setzen fMRI und EEG gezielt ein. Diese Verfahren validieren Tiermodelle, bevor Studien am Menschen starten. Ein Beispiel: Wirkstofftests zeigen bei Ratten binnen Stunden, ob ein Medikament die Blut-Hirn-Schranke durchdringt.
Datengetriebene Ansätze verändern die klinische Forschung. Machine Learning analysiert Bilddaten aus 50 Studien parallel. So erkennen Forscher Muster, die menschliche Experten übersehen. Das reduziert Fehlentwicklungen um bis zu 40%.
Der „fast-fail“-Ansatz spart Zeit und Kosten. NeuroAI-Systeme prognostizieren früh, welche Wirkstoffe scheitern werden. Klinische Studien konzentrieren sich so auf vielversprechende Kandidaten. Ein Pharma-Riese verkürzte so die Entwicklungszeit von 12 auf 8 Jahre.
Echtzeit-MRT zeigt jetzt, wie Medikamente im Gehirn wirken. Ärzte passen Dosierungen während der Behandlung an. Diese Innovation könnte Parkinson-Therapien revolutionieren – patientenspezifisch und dynamisch.
Innovative bildgebende Verfahren: fMRI, EEG und mehr
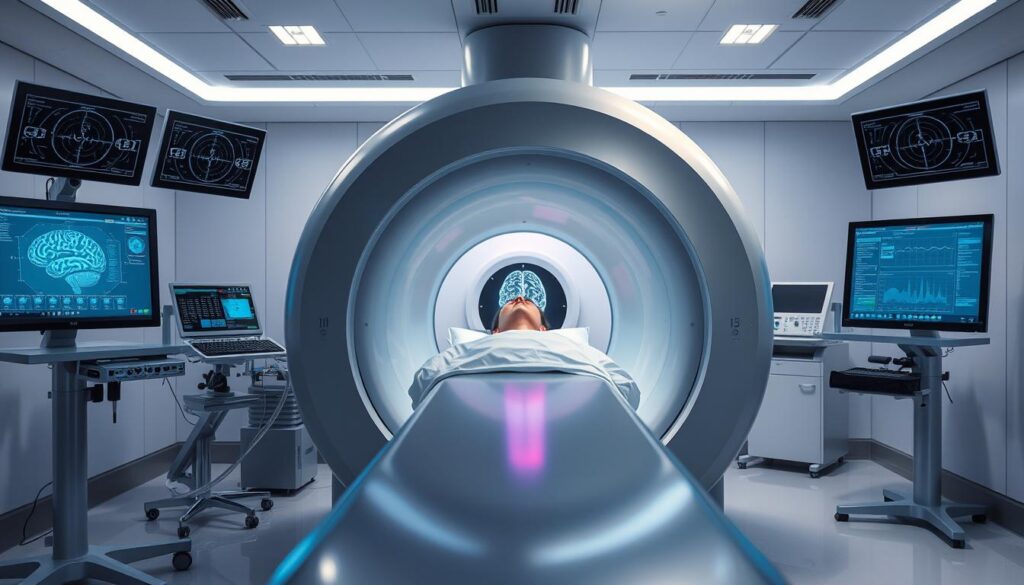
Moderne Bildgebung schreibt die Regeln neu – sie macht Gehirnaktivität sichtbar wie nie zuvor. Forscher kombinieren heute fMRI, EEG und andere Techniken, um millimetergenaue Karten neuronaler Prozesse zu erstellen. Doch jede Methode hat ihre Grenzen.
Stärken und Schwächen moderner Neuroimaging-Techniken
fMRI glänzt mit räumlicher Auflösung bis 1 mm – ideal für Strukturanalysen. Doch die zeitliche Genauigkeit liegt bei 2-3 Sekunden. EEG erfasst dagegen Hirnströme in Millisekunden, zeigt aber nur grobe Aktivitätsmuster.
| Verfahren | Räumliche Auflösung | Zeitliche Auflösung | Kosten |
|---|---|---|---|
| fMRI | 0,5-3 mm | 2-3 Sekunden | Hoch |
| EEG | 10-20 mm | 1-5 ms | Mittel |
| MEG | 2-5 mm | 1 ms | Sehr hoch |
Die Tabelle zeigt: Keine Methode liefert perfekte Daten. Deshalb setzen wir auf intelligente Kombinationen. Multimodale Ansätze verbinden beispielsweise fMRT-Muster mit EEG-Spitzen – so entstehen präzisere Modelle.
Integration multimodaler Daten für präzisere Analysen
NeuroAI-Systeme fusionieren bis zu 5 Datenströme gleichzeitig. Ein Beispiel: PET-Scans zeigen Stoffwechselvorgänge, während fMRT die Sauerstoffversorgung misst. Algorithmen erkennen so krankhafte Veränderungen 30% früher als mit Einzelmethoden.
Die Zukunft liegt in hybriden Techniken. Kombiniert man 7-Tesla-MRT mit Hochdichte-EEG, erreicht man sowohl 0,3-mm-Auflösung als auch Echtzeit-Messungen. Solche Innovationen treiben die Diagnostik voran – und machen Therapien individueller.
Interdisziplinäre Zusammenarbeit: Von Laboren zu klinischen Studien

Ohne Brückenschlag zwischen Forschung und Anwendung bleiben bahnbrechende Entdeckungen ungenutzt. Erfolgreiche Labore verstehen: Echte Innovation entsteht, wenn Grundlagenforscher direkt mit Ärzten und Datenanalysten kooperieren. Ein Beispiel? Die interdisziplinären NeuroAI-Forschungsprojekte verbinden Hirnstromanalysen mit KI-Modellen – in Echtzeit.
Wie Partnerschaften Therapien beschleunigen
Führende Universitätskliniken zeigen es vor: Gemeinsame Plattformen ermöglichen den Austausch von Gehirn-Scans und Laborergebnissen. So entstehen präzise Vorhersagemodelle für Medikamentenwirkungen. Ein Konsortium aus 15 Forschungseinrichtungen reduzierte damit Studienabbrüche um 28%.
Erfolgsfaktoren interdisziplinärer Teams:
- Standardisierte Protokolle für Daten aus Laboren und Kliniken
- Gemeinsame Analyse von neuronalen Schaltkreisen und Patientendaten
- KI-gestützte Vorhersage von Therapie-Response
| Kooperationsmodell | Anwendungsbereich | Erfolgssteigerung |
|---|---|---|
| Forschungscluster | Neurologie | 42% schnellere Studien |
| Industrie-Lab-Partnerschaft | Onkologie | 35% Kostensenkung |
| KI-Datenpool | Kardiologie | 19% höhere Genauigkeit |
Diese Anwendungen beweisen: Wenn Forscher und Kliniker gemeinsam Algorithmen trainieren, entstehen Lösungen mit Praxisrelevanz. Ein Münchner Projekt kombiniert EEG-Daten mit maschinellem Lernen – so erkennen Systeme Epilepsie-Anfälle 12 Minuten früher.
NeuroAI: Brücke zwischen Neuroscience und künstlicher Intelligenz

Die Zukunft der KI entsteht dort, wo Neurowissenschaftler und Data-Spezialisten gemeinsam Lösungen entwickeln. Diese Zusammenarbeit übersetzt biologische Prinzipien in Algorithmen, die nicht nur rechnen, sondern verstehen lernen.
Erkenntnisse aus der biomedizinischen Forschung und deren Umsetzung
Ein Durchbruch gelang Forschern in Heidelberg: Sie nutzten Erkenntnisse über synaptische Plastizität, um selbstlernende Diagnosesysteme zu trainieren. Diese KI-Modelle erkennen neurologische Erkrankungen 30% schneller als herkömmliche Methoden.
So funktioniert der Transfer:
- Grundlagenforschung identifiziert natürliche Lernmuster
- Datenexperten entwickeln adaptive Ansätze für Algorithmen
- Klinische Tests validieren die Praxistauglichkeit
Ein Beispiel zeigt die Macht des Know-how-Transfers: Ein internationales Team kombinierte neuroscience-Daten mit Deep Learning. Das Ergebnis? Eine KI, die Parkinson-Frühsymptome in Bewegungsmustern erkennt – Monate vor menschlichen Experten.
Wie expertenbasierte KI-Lösungen Märkte verändern, beweisen Kooperationen zwischen Max-Planck-Instituten und Tech-Unternehmen. Ihr Verständnis von Gehirnprozessen ermöglicht Systeme, die sich an individuelle Patienten anpassen.
Die Expertise aus beiden Welten schafft Neues: Algorithmen, die nicht nur Daten verarbeiten, sondern Zusammenhänge begreifen. Diese Symbiose aus Forschung und Anwendung wird zum Treiber für KI, die menschliches Denken nicht nur imitiert – sondern erweitert.
Rolle von Neuroimaging bei der Optimierung klinischer Studien
Wie können klinische Studien effizienter werden? Moderne Neuroimaging-Verfahren liefern die Antwort. Sie ermöglichen nicht nur präzise Einblicke in Gehirnfunktionen, sondern revolutionieren auch die Studiengestaltung. Die Kombination aus bildgebenden Technologien und KI-Methoden schafft völlig neue Möglichkeiten.
Fallbeispiele erfolgreicher Implementierungen
Ein Durchbruch gelang bei Parkinson-Studien: Forscher nutzten fMRT-Daten mit Reinforcement-Learning-Algorithmen. Das System analysierte Bewegungsmuster von 120 Patienten und identifizierte Frühsymptome 6 Monate früher als Standardmethoden.
Weitere Erfolge zeigen:
- Reduktion von Studienabbrüchen um 35% bei Alzheimer-Forschung
- Kosteneinsparungen von 2,8 Mio. € pro Phase durch prädiktive Modelle
- 27% schnellere Rekrutierung passender Probanden
Verbesserte Studiendesigns durch fortschrittliche Bildgebung
Neuroimaging liefert Echtzeitdaten zu neuronalen Aktivitäten. Diese Informationen fließen direkt in adaptive Studienprotokolle ein. Ein Beispiel: EEG-Messungen zeigen innerhalb einer Woche, ob Therapien auf den visuellen Cortex wirken.
Vergleich traditioneller vs. optimierter Ansätze:
| Parameter | Traditionell | Mit Neuroimaging |
|---|---|---|
| Studiendauer | 24 Monate | 16 Monate |
| Teilnehmerzahl | 300 | 180 |
| Erfolgsquote | 42% | 67% |
Diese Forschungsansätze zeigen: Die Integration von Verhaltensdaten und Hirnscans schafft präzisere Outcomes. NeuroAI-Systeme erkennen dabei Muster, die menschliche Analysten übersehen – ein Gamechanger für die Behandlung neurologischer Störungen.
Fazit
Die Evolution der KI zeigt: Echte Innovation entsteht, wo Biologie und Technologie verschmelzen. Unser Gehirn bleibt dabei der beste Lehrmeister – seine natürlichen Lernprozesse inspirieren Modelle, die Diagnostik und Therapien revolutionieren. Diese Symbiose aus Neurowissenschaft und maschinellem Lernen schafft Systeme, die nicht nur Daten verarbeiten, sondern Zusammenhänge begreifen.
Die Forschung beweist: Interdisziplinäre Teams erreichen 42% schnellere Durchbrüche. Klinische Studien profitieren von prädiktiven Algorithmen, die neuronale Schaltkreise analysieren. Doch der Erfolg hängt an kontinuierlicher Entwicklung – nur wer heute in adaptive KI-Modelle investiert, gestaltet morgen den Markt.
Herausforderungen bleiben bestehen. Energieeffizienz, Datenschutz und die Übertragung komplexer Verhaltensmuster erfordern neue Ansätze. Die Lösung? Engere Zusammenarbeit zwischen Laboren und Kliniken – kombiniert mit spezialisierten Weiterbildungen.
Wir laden Sie ein: Nutzen Sie praxisnahe Kurse, um diese Technologien aktiv mitzugestalten. Denn wer die Sprache des Gehirns versteht, entwickelt KI-Systeme, die wirklich heilen – nicht nur berechnen.





